緊急時とはいえ、安全性についてまだ不確定な部分がある新型インフルエンザワクチンですが、厚労省では、新型インフルエンザワクチン接種後の副作用報告については、メーカーによる報告だけではタイムラグなどがあることから、接種を委託する医療機関に直接依頼することを検討しています。(委託契約の条件)
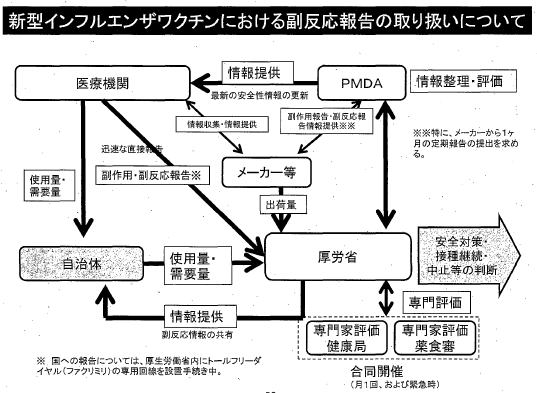
(2009年10月2日開催 新型インフルエンザ対策担当課長会議の参考資料 より引用)
これに対し、米国では1970年代の豚インフルエンザワクチンの悪夢があってか、従来からあるオンラインでも可能な副作用報告システム(患者やその家族なども可)に加え、接種者に連絡先カードを配る、大学による接種者へのメールモニター実施など、副作用を収集するためにあらゆる手段が講じられると伝えられています。
ガッチリ監視、副作用(米)(新型インフルエンザ・ウォッチング日記 2009年9月28日)
http://blog.goo.ne.jp/tabibito12/e/f508fcce2870326088e3b71e55edc417
Intense hunt begins for new shot’s side effects
(MSNBC 2009.9.27 AP配信 おそらく上記の引用記事)
http://www.msnbc.msn.com/id/33045346/ns/health-swine_flu
Vaccine Adverse Event Reporting System (VAERS)
http://vaers.hhs.gov/index
上記のような、ワクチンの接種者やその家族が直接副作用報告ができるシステムは、医薬品の副作用直接報告システム同様、英国やカナダなどでも実施されています。
厚労省では接種が始まる今月中旬までに専用のファクス回線を準備したり、委託医療機関以外にも、都道府県や市町村を通じて協力を呼びかけるとしていますが、果たして感染拡大時に症例の把握が十分行うことができるでしょうか?
ワクチンは、接種後医療機関に効果判定のために訪れることはまずないのですから、子宮頸がん予防ワクチンの例が示すように、患者などが直接報告できる仕組みの検討や、米国のような、より細かい把握の仕組みを検討する必要はないのでしょうか?
関連サイト:
Influenza A (H1N1) 2009 Monovalent Vaccine Safety Monitoring(FDA)
http://www.fda.gov/BiologicsBloodVaccines/SafetyAvailability/VaccineSafety/ucm182290.htm
Influenza A (H1N1) 2009 Monovalent Vaccine Safety Monitoring: CDC Planning Recommendations for State, Local, Tribal, and Territorial Health Officials(CDC)
http://www.cdc.gov/h1n1flu/vaccination/safety_planning.htm
関連情報:TOPICS
2009.09.11 HPVワクチンに関する情報
2009.08.22 子宮頸がん予防ワクチンと有害事象
参考:読売新聞10月4日
http://www.yomiuri.co.jp/iryou/news/iryou_news/20091004-OYT8T00213.htm
2009年10月05日 01:07 投稿

薬剤師さん全員が 報告をするべく 行動して欲しいものです。世間話で終わらせずに。
事実報告で構わないのですから。こんな時に 日薬はフォーマットを作って 会員薬局に配布するべきではないのでしょうか。
ワクチン接種できない患者(卵アレルギー)もいることを念頭に パンデミックな言葉や反応は慎みたいものです。とにかく感染したら 外出しない。これが基本。近隣の薬局間の繋がりがここで機能します。在庫薬を感染していない薬局に移動すれば 地域でなんとか制御できるはずです。
高い社会性が判断どころだと思います。
早急に考えるのは トリアージ。医療者だからこそ 冷静に判断できる意志を持ちたいですね。
接種方法が異なるということもありますが、海外ではワクチン接種を地域薬局で行うということもありますから、薬剤師によるワクチン接種に関する副作用報告への取り組みはおそらく行われているのでしょうね。
ワクチン接種後、吐き気や下痢などの症状を訴えて薬局に相談に来るかもしれませんから、日本でも組織的な取り組みもあってもいいですね。